アロステム®シート学術情報/
臨床試験データ
「警告・禁忌を含む注意事項等情報」などは電子添文をご参照ください。
国内第Ⅲ相試験(ISN001-EB-02)1)
- 1)承認時評価資料:国内第Ⅲ相試験(ISN001-EB-02)社内資料
本試験は、イシンファーマ株式会社からの資金提供による支援を受けている。
目的
表皮水疱症患者を対象に、治療前観察期間の平均潰瘍面積に対する潰瘍面積平均変化率の評価によりヒト(同種)脂肪組織由来間葉系幹細胞(ALLO-ASC)シートの有効性を検証し、安全性を検討する。
試験デザイン
多施設共同、非盲検、単群、国内第Ⅲ相試験
対象
厚生労働省の指定難病診断基準2)により診断された栄養障害型表皮水疱症、接合部型表皮水疱症または単純型表皮水疱症(重症汎発型に限る)患者
- 栄養障害型:6例[FASおよび安全性解析対象集団]a)
- それ以外の病型[接合部型および単純型(重症汎発型に限る)]:0例
- a)1例はフォローアップ調査期間中の最終貼付34週後の評価後に患者からの申し出により試験を中止した。
- FAS:最大の解析対象集団
方法
治療前観察期間(4週間)、治療期間(最大12週間)、後観察期間(5週間)、追跡観察期間(20週間)及びフォローアップ調査期間(27週間)より構成され、治験参加期間は最大68週間であった。本品を治療期間中[治療開始日(Visit3)、Visit4-1~4-20]、原則週1回の頻度で、皮膚潰瘍とその周辺を含め十分に覆うように必要な枚数(16枚以内)を最大12回貼付した。ただし、治療開始から3回(3週)貼付を繰り返しても顕著な潰瘍面積の縮小が認められない場合、週2回の貼付を可能としb)、12週で最大計21回(1回×3週+2回×9週)の貼付とした。なお、治療期間中は初回貼付時に使用した貼付枚数を変更せず、1回あたりの使用枚数を固定した。
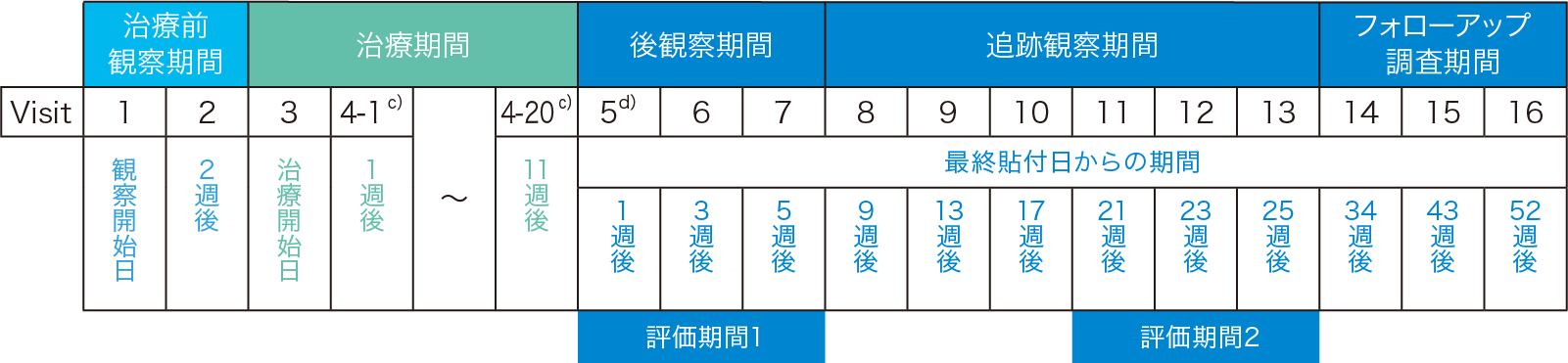
- b)本試験では週2回の貼付を行った患者はいなかった。
- c)Visit4は、各患者の貼付回数により異なり、4-1(2回貼付)から最大4-20(21回貼付)とした。同一患者において複数の貼付領域に本品を貼付する場合は、すべての領域の貼付が終了するまで、表皮化を認めた貼付領域も含め継続して貼付を行うこととした。Visit4-2~Visit4-19ではVisit4-20と同様の調査・観察項目を実施した。
- d)Visit5の来院は、同一患者における本品の最終貼付から1週後の日とした。
評価項目
有効性
主要評価項目:
- 治療前観察期間の平均潰瘍面積に対する評価期間1の潰瘍面積平均変化率(検証的解析項目)
- 治療前観察期間の平均潰瘍面積に対する評価期間2の潰瘍面積平均変化率(検証的解析項目)
副次評価項目:
- 貼付領域に存在する皮膚潰瘍の表皮化(完全閉鎖)および潰瘍面積が50%縮小するまでの期間
- 貼付領域における皮膚潰瘍の縮小効果が持続する期間(累計値として)
- VAS(疼痛、そう痒感:観察開始日~最終貼付25週後の期間中毎日、貼付領域について計測)の変化量 など
- VAS:視覚的アナログ尺度
安全性
副作用
解析計画
有効性
FASを対象として解析を行った。主要評価項目について、患者ごとに治療前観察期間の平均潰瘍面積に対する評価期間1(最終貼付1、3および5週後)の潰瘍面積平均変化率(%)を算出した。栄養障害型の患者の潰瘍面積平均変化率が統計学的に0と異なることについて、1標本t検定を行い、0との有意差が検出されたことをもって、本試験の有効性達成基準を満たすものとした。有意水準は両側5%とした。評価期間1と同様に、治療前観察期間の平均潰瘍面積に対する評価期間2(最終貼付21、23および25週後)の潰瘍面積平均変化率(%)を算出した。栄養障害型の患者において評価期間1で有意な差が認められた場合に、評価期間1と評価期間2の潰瘍面積平均変化率の平均値の差およびその95%信頼区間を算出し、評価期間1と評価期間2を比較した。副次評価項目については、データに応じて要約統計量(例数、平均値、標準偏差、最小値、最大値、95%信頼区間、または例数、中央値、四分位範囲)を算出した。
安全性
SASを対象として解析を行った。有害事象の要約として、MedDRA/J v27.1を用いて読み替えた有害事象を、器官別大分類および基本語で定義された事象別に発現割合を集計した。また、重篤な有害事象、本品と関連のある有害事象、重篤な本品と関連のある有害事象も事象別に発現割合を集計した。
- MedDRA/J:ICH国際医薬用語集日本語版
有効性
治療前観察期間の平均潰瘍面積に対する評価期間1の潰瘍面積平均変化率【主要評価項目、検証的解析結果】
治療前観察期間の平均潰瘍面積に対する評価期間2の潰瘍面積平均変化率【主要評価項目、検証的解析結果】
治療前観察期間(貼付前4週、2週および貼付直前)の平均潰瘍面積に対する評価期間1(最終貼付1、3および5週後)の潰瘍面積平均変化率±標準誤差は−54.242±13.3863%であり、統計学的に有意な潰瘍面積の縮小が認められ(p=0.0098、1標本t検定)、有効性達成基準を満たした。治療前観察期間の平均潰瘍面積に対する評価期間2(最終貼付21、23および25週後)の潰瘍面積平均変化率±標準誤差は−29.853±18.8147%であった。
| 栄養障害型(n=6) | ||
|---|---|---|
| 治療前観察期間に対する評価期間1の潰瘍面積 | 平均変化率、% | -54.242 |
| 標準誤差 | 13.3863 | |
| t値a) | -4.05 | |
| p値a) | 0.0098 | |
| 治療前観察期間に対する評価期間2の潰瘍面積 | 平均変化率、% | -29.853 |
| 標準誤差 | 18.8147 | |
| 潰瘍面積平均変化率の差b) 評価期間2-評価期間1 |
平均変化率の差、% | 24.389 |
| 95%信頼区間 | -2.5103~51.2888 | |
- a)帰無仮説を「潰瘍面積平均変化率(%)の平均が0である」としたときの1標本t検定
- b)評価期間1において統計的に有意な差が認められた場合のみ、評価期間2と評価期間1の差に関する集計を行うこととした。
- 評価期間1:最終貼付1、3及び5週後、評価期間2:最終貼付21、23及び25週後
個々の患者の治療前観察期間に対する各測定時点の潰瘍面積変化率の推移を以下に示す。
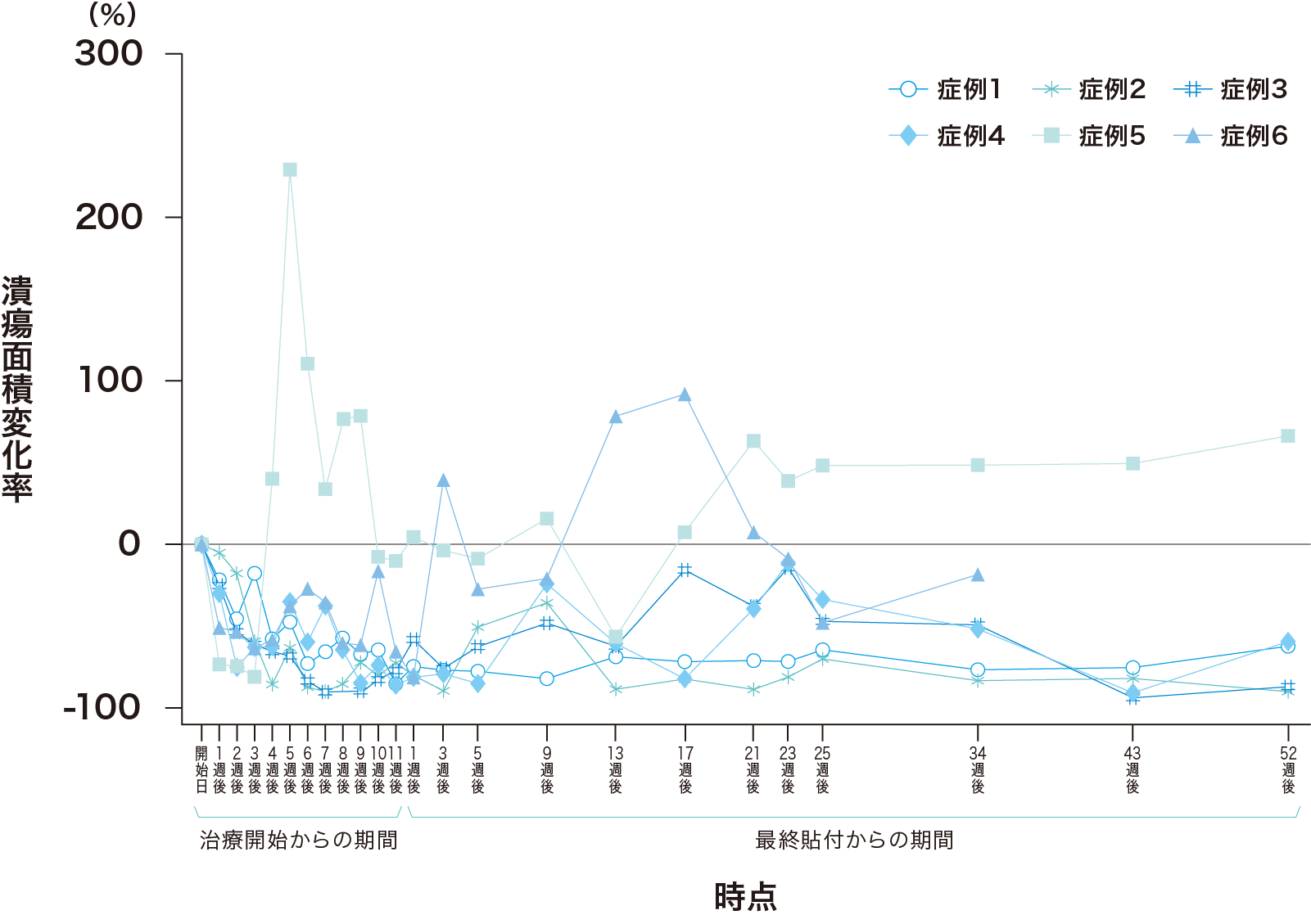 拡大図を表示する
拡大図を表示する
貼付領域に存在する皮膚潰瘍の表皮化(完全閉鎖)および潰瘍面積が最初に50%縮小するまでの期間【副次評価項目】
貼付領域の皮膚潰瘍に表皮化(完全閉鎖)が認められた患者はいなかった。潰瘍面積の50%縮小は6例中6例に認められ、潰瘍面積が最初に50%縮小するまでの期間の中央値(Q1~Q3)は17.5日(15.0~22.0)であった。
| 栄養障害型(n=6) | ||
|---|---|---|
| 潰瘍面積が最初に50%縮小するまでの期間、日 | 中央値 | 17.5 |
| Q1, Q3 | 15.0, 22.0 | |
| 四分位範囲 | 7 | |
貼付領域における皮膚潰瘍の縮小効果が持続する期間(累計値として)【副次評価項目】
全6例の皮膚潰瘍の観察期間中央値(Q1~Q3)は、442.0(435.0~442.0)日であった。試験期間中、治療前観察期間からの25%および50%以上の潰瘍面積の縮小は全6例で認められ、持続累計期間中央値(Q1~Q3)はそれぞれ、413.5(174.0~427.0)日および298.5(35.0~406.0)日であった。
| 栄養障害型(n=6) | ||
|---|---|---|
| 治療前観察期間の潰瘍面積平均より下回っている期間、日 | 中央値 | 432.5 |
| Q1, Q3 | 258.0, 435.0 | |
| 四分位範囲 | 177 | |
| 25%以上縮小している期間、日a) | 中央値 | 413.5 |
| Q1, Q3 | 174.0, 427.0 | |
| 四分位範囲 | 253 | |
| 50%以上縮小している期間、日a) | 中央値 | 298.5 |
| Q1, Q3 | 35.0, 406.0 | |
| 四分位範囲 | 371 | |
| 皮膚潰瘍の観察期間、日 | 中央値 | 442.0 |
| Q1, Q3 | 435.0, 442.0 | |
| 四分位範囲 | 7 | |
- a)治療前観察期間における潰瘍面積平均から25%以上、50%以上縮小している期間とする。条件を満たした時点から、条件から外れたことが確認された最初の時点までを集計対象期間とする。ただし、条件を満たしている期間に未測定日が含まれる場合は、累計値には含まない。
参考情報 VAS(疼痛、そう痒感:観察開始日~最終貼付25週後の期間中毎日、貼付領域について計測)の変化量
【副次評価項目】
疼痛
観察開始日と比較して、本品貼付開始1週以降のVAS値の変化量の平均値が2を超える減少はいずれの時点でも認められなかったが、最終貼付5、9、13、17週後に約1減少し、この4時点の変化量の平均値の95%信頼区間の上限は0を下回った。
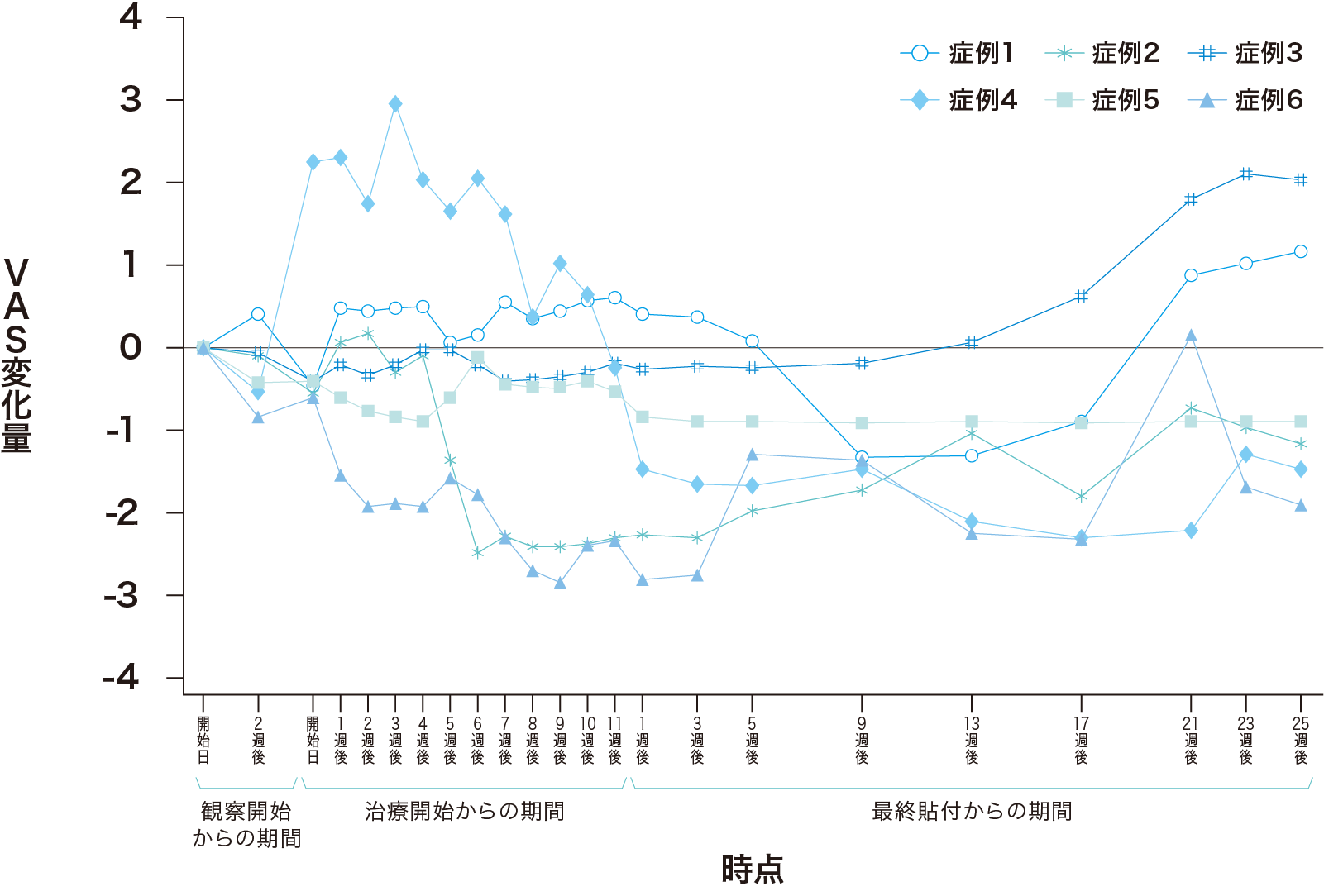 拡大図を表示する
拡大図を表示する
そう痒感
観察開始日と比較して、貼付開始1週以降のVAS値の変化量の平均値が2を超える減少は最終貼付3、5、9、13、17週後に認められ、これら5時点の変化量の平均値の95%信頼区間の上限は0を下回った。
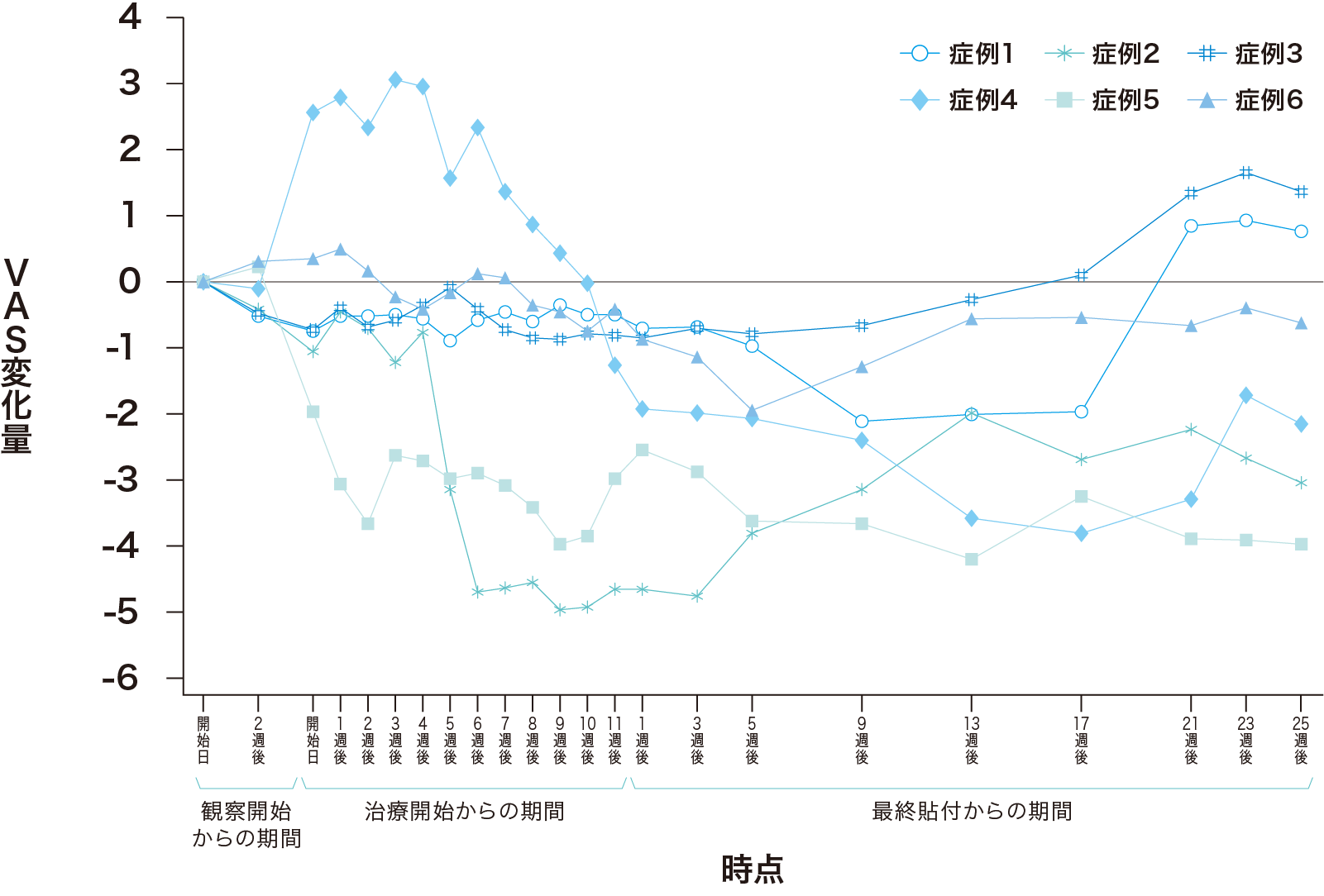 拡大図を表示する
拡大図を表示する
安全性
副作用(安全性解析対象集団)
副作用は6例中1例に認められ、C反応性タンパク上昇(重症度:軽度)であった。重篤な副作用、貼付中止に至った副作用、死亡に至った副作用は認められなかった。
- ※アロステム®シートの国内臨床試験結果の詳細は、総合製品情報概要、インタビューフォームなどをご参照ください。
参考文献
- 1)承認時評価資料:国内第Ⅲ相試験(ISN001-EB-02)社内資料
本試験は、イシンファーマ株式会社からの資金提供による支援を受けている。 - 2)厚生労働省.指定難病一覧(令和7年4月1日施行).表皮水疱症(指定難病36)
- 監修
- 石河 晃(いしこう あきら)先生
東邦大学 皮膚科学 表皮水疱症再生治療学講座 教授